| 状态: | |
|---|---|
| 数量: | |
临床相关 ——概括人类 CLE 与光敏性皮肤损伤、TLR7 通路激活和自身抗体产生。
机制驱动 ——TLR-7激动剂驱动先天免疫激活; UVB 会诱导细胞损伤和 IFN-α 产生,协同诱导 CLE 病理。
综合终点 ——皮肤临床评分、血清抗 dsDNA 抗体、皮肤 IFN-α 水平、组织病理学 (HE)、皮肤 RNA-seq 转录组学、免疫细胞聚类分析。
转化价值 – 非常适合测试局部和全身免疫调节剂、JAK 抑制剂、抗 IFNAR 生物制剂(anifrolumab)和 TLR 通路抑制剂。
IND 就绪数据包 ——可以根据 GLP 原则进行研究。
TLR-7激动剂+UVB诱导的NHP CLE模型
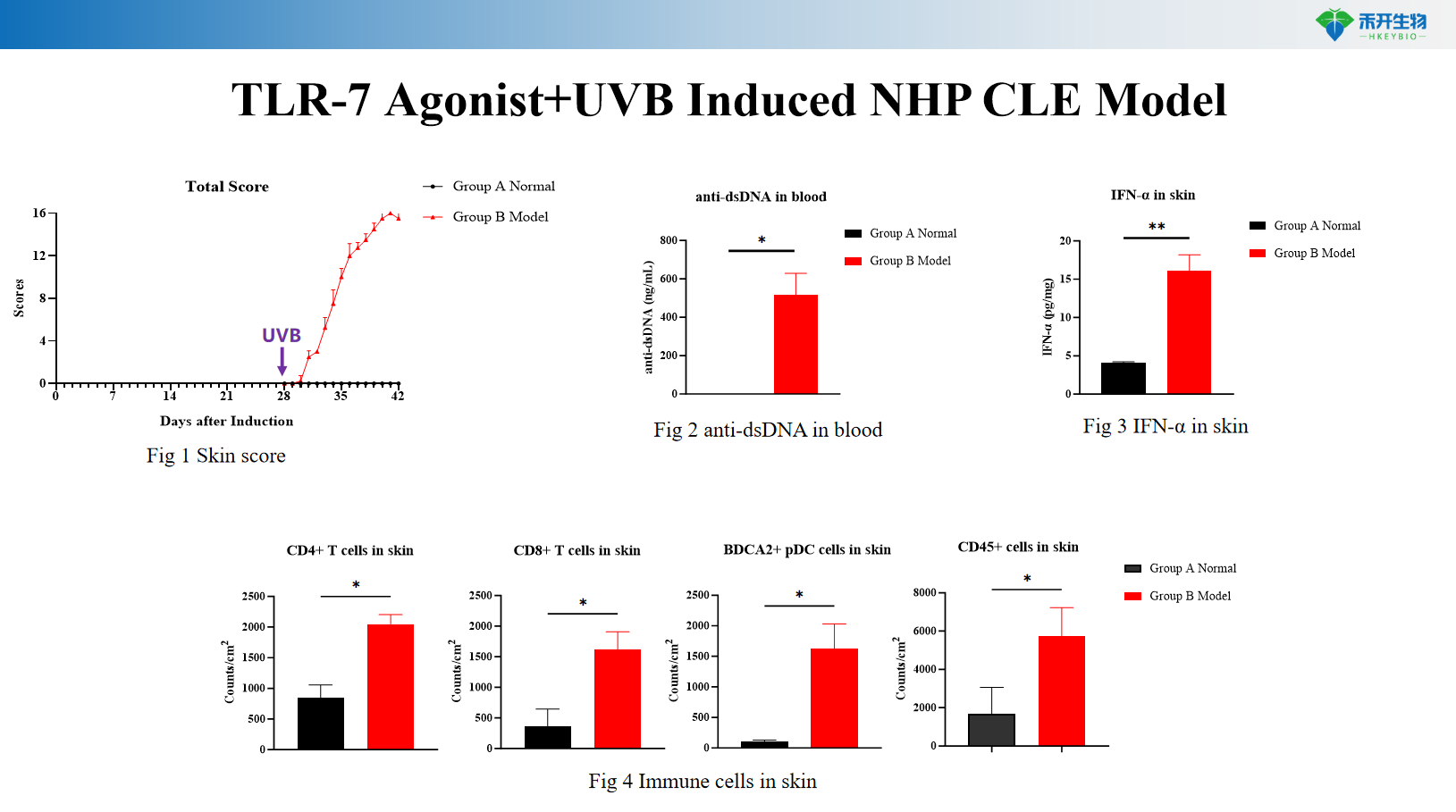
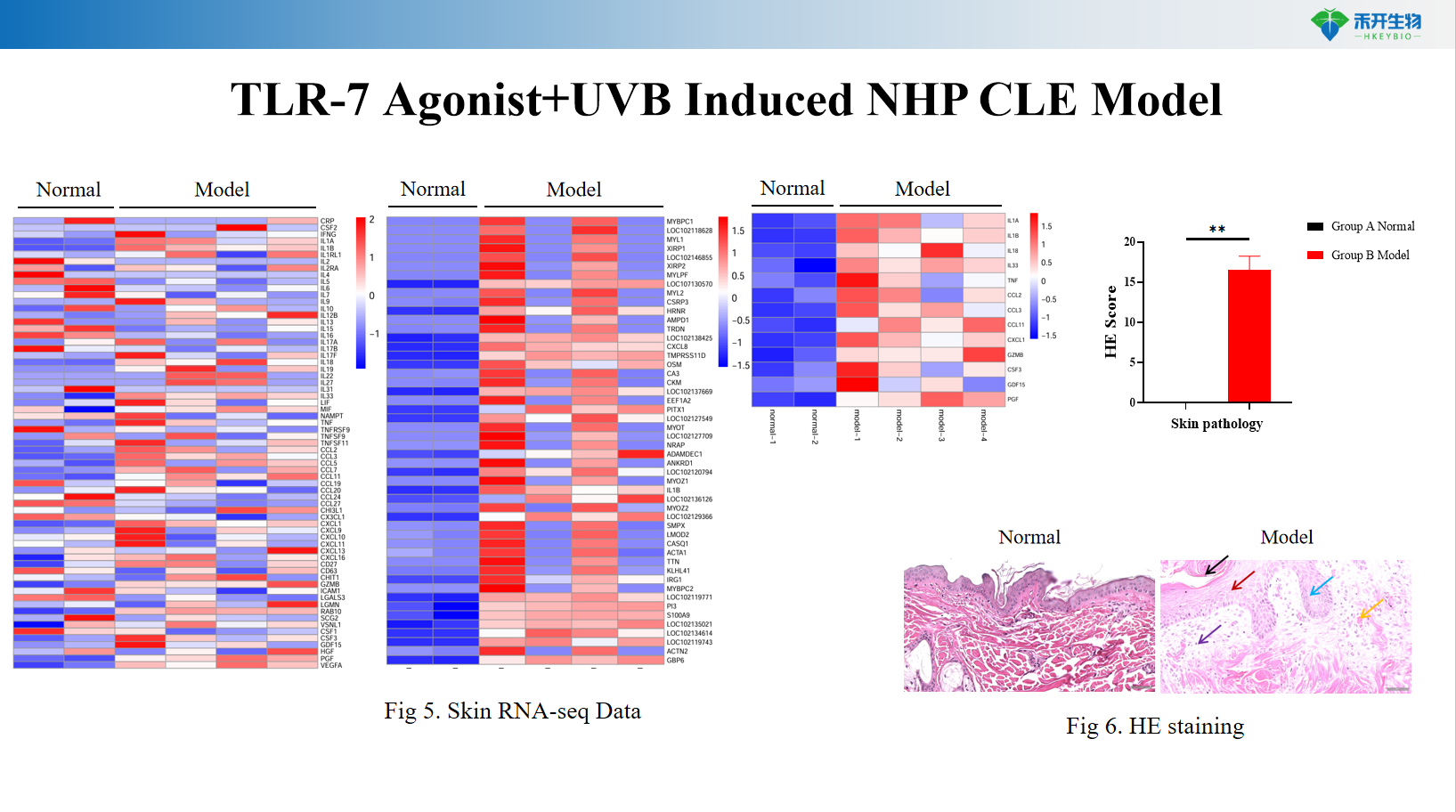
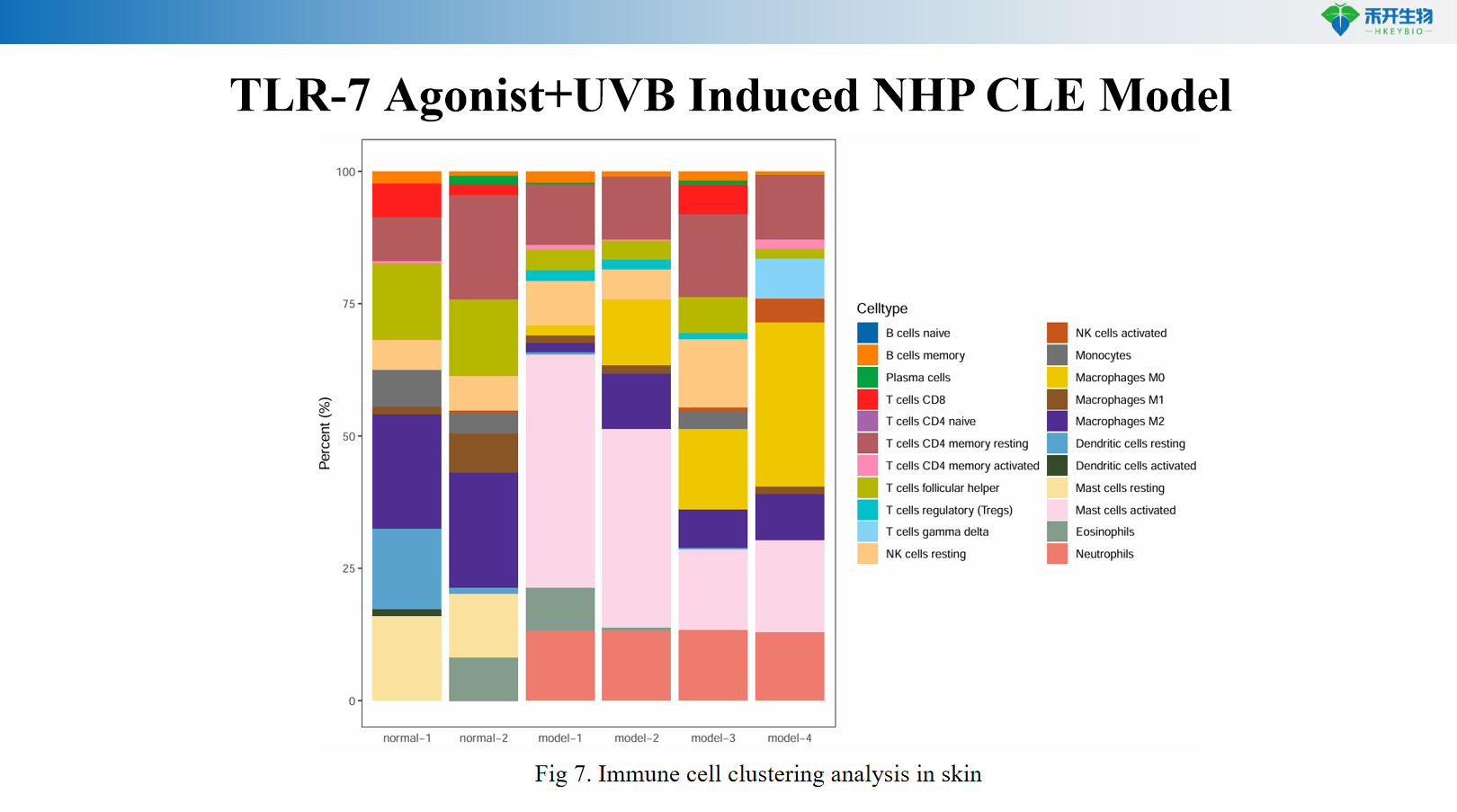
• 局部和全身免疫调节剂(皮质类固醇、钙调神经磷酸酶抑制剂、JAK 抑制剂)的功效测试
• 针对 I 型干扰素(anifrolumab)、TLR7/8 通路和 B 细胞(利妥昔单抗)的生物制剂的评估
• 光敏自身免疫途径的目标验证
• 生物标志物发现(抗 dsDNA、IFN-α、皮肤转录组特征)
• 支持 IND 的药理学和毒理学研究
范围 | 规格 |
物种/品系 | 食蟹猴 ( Macaca fascicularis ) |
感应法 | 将局部 TLR-7 激动剂(例如咪喹莫特)涂抹在剃光的背部皮肤上 + UVB 照射(312 nm,多次曝光) |
学习时间 | 2–4 周(诱导+治疗阶段) |
关键终点 | 皮肤临床评分(红斑、鳞屑、增厚)、血清抗 dsDNA 抗体 (ELISA)、皮肤 IFN-α 水平 (ELISA/qPCR)、皮肤组织病理学(HE 评分)、皮肤 RNA-seq 转录组学、免疫细胞聚类分析(流式细胞术/scRNA-seq) |
数据包 | 原始数据、分析报告、临床照片、组织学切片、RNA-seq数据、生物信息学分析 |
问: 为什么将 TLR-7 激动剂与 UVB 结合用于 CLE 诱导?
答: TLR-7 激动剂激活先天免疫途径,而 UVB 则诱导细胞损伤和 IFN-α 产生。该组合协同概括了人类 CLE 的复杂发病机制,包括光敏性和 I 型干扰素特征。
问: 与人类 CLE 的主要相似之处是什么?
答: 该模型表现出光敏性皮肤损伤、抗 dsDNA 抗体升高、皮肤中 IFN-α 上调以及与人类 CLE 相似的组织病理学变化(表皮增生、炎症浸润)。
问: 该模型可以用于 IND 支持研究吗?
答: 是的。研究可以根据监管提交(FDA、EMA)的 GLP 原则进行。
问: 你们是否提供定制研究方案(例如,不同的 TLR-7 激动剂剂量、UVB 暴露方案)?
答: 当然。我们的科学团队为您的特定候选药物量身定制诱导方案、治疗计划和终点分析。
问: 试点功效研究的典型时间表是怎样的?
答: 研究通常在 4 周内完成,包括诱导、治疗和综合终点分析。
内容为空!
